News
2019年4月16日の米国政府からの『腹圧性尿失禁を治療する手術を検討している場合』とするよびかけ
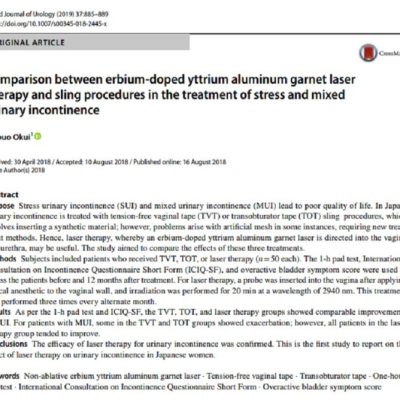
2010年に実行された腹圧性尿失禁手術SUIのおよそ250,000例について調査した注意が発表されました。
女性のSUI用ミニスリングの安全性と有効性は十分に実証されていないことを示しました。
SUIのメッシュスリング手術は、女性の報告と身体検査に基づいて、1年で女性の約70〜80%で成功していると報告されています。
経膣SUI修復でメッシュスリングを使用すると、SUI修復の従来の非メッシュ手術には存在しないリスクが生じます。これは、メッシュ露出です。
SUI修復用の外科用メッシュスリングの報告される最も一般的な合併症には、頻度の高い順に:痛み、膣のメッシュ侵食(露出、突出または突出とも呼ばれます)、感染、尿の問題、再発性失禁、痛み性交(性交疼痛症)、出血、臓器穿孔、神経や筋の問題および膣の瘢痕。これらの合併症の多くは追加の医学的介入を必要とし、時には外科的治療および/または入院を必要とします。以上は、メッシュを使わない場合には生じない合併症と考えることができます
骨盤臓器脱を修復治療するためこの数年間は、ポリプロピレンという材質でできた人工メッシュを使います。これには、3種類あります。1.骨盤臓器脱のための経膣人工メッシュ(TVM)、2.骨盤臓器脱のための経腹人工メッシュ(LSC)、3.腹圧性尿失禁のための人工メッシュスリング(TOT,TVT)です。このうち1の経膣メッシュは認可して時間がたちましたので、米国政府が見直しに入りました。すると副作用が強く苦痛に悩んでいる女性が多いことがわかりました。この経膣人工メッシュ(TVM)の術中合併症として、膀胱損傷、尿管損傷、直腸損傷、出血が挙げられます。また、術後合併症としては、感染、人工メッシュびらん・露出・周辺臓器への露出、慢性的な疼痛、排尿障害などが挙げられます。
そこで、まず、2011年7月13日に米国FDA(Food and Drug Administration:食品医薬品局)の注意喚起がありました。FDAが、最新の科学文献に記載された有害事象や合併症の分析に基づくFDAの安全性評価結果を医療機関と患者に知らせるためのもので、2回にわかりおこなわれました。その内容は以下のようにまとめることができます。
「骨盤臓器のための経膣人工メッシュ手術(TVM)に関連する重大な合併症」
1. 骨盤臓器脱の経膣修復のための人工メッシュ(TVM)手術に関連する重大な合併症はまれではない。
2.人工メッシュを用いた経膣的骨盤臓器脱修復(TVM)が従来の人工メッシュを使わない修復よりも効果的であることは明らかではない
しかし、それだけでは骨盤臓器脱の修復手術としてのメッシュの問題は解決しませんでした。そこで、2019年にFDAは大きな決断をすることになりました。
2019年4月16日、FDAは骨盤臓器脱に対する経腟メッシュ手術に使用する外科用メッシュのすべての製造業者に、自社製品の販売と流通を直ちに中止するよう命じました。今回は、メッシュを製造するメーカーに対して、もともと手術糸として登録していたのを、インプラントとして格上げを要求しました。しかし、メーカーはこの要求に応じメッシュの製造はおわりました。こうして、膣メッシュは米国では事実上実施することができなくなったのです。
腹圧性尿失禁や骨盤臓器脱への人工メッシュ手術の安全性 2016年12月20日のスコットランドで尿失禁手術約1万7,000例、骨盤臓器脱手術約1万9,000例のコホート研究を実施され、主要評価項目は、手術直後の合併症、術後の合併症による入院(5年以内)、さらなる尿失禁手術または骨盤臓器脱手術で、以下の結果が示されました。(医学雑誌Lancetに「腹圧性尿失禁や骨盤臓器脱への人工メッシュ手術の安全性」2016年)
腹圧性尿失禁に対しては、人工メッシュ手術が支持されました。しかし推奨ではありません。
骨盤臓器脱のうち膀胱がおちる『前膣壁脱』および直腸が落ちる『後膣壁脱』に対しては、単独で最初の手術として行う場合、人工メッシュ手術は推奨されないとしました。つまり、初対面の患者さんに対して、いきなりメッシュを勧めることの患者メリットがないとしたのです。 骨盤臓器脱手術に関しては、経膣および経腹(腹腔鏡)人工メッシュ手術はいずれも、経膣非メッシュ手術との比較において有効性および合併症は同程度でした。つまり、メッシュなしの手術も、ありの手術も、かわりないわけです。ここでもあえて、メッシュを優先する必要はないと考えます。